Nat Med | Μια πολυ-ομική προσέγγιση για τη χαρτογράφηση του ολοκληρωμένου όγκου, του ανοσοποιητικού και του μικροβιακού τοπίου του καρκίνου του παχέος εντέρου αποκαλύπτει την αλληλεπίδραση του μικροβιώματος με το ανοσοποιητικό σύστημα
Παρόλο που οι βιοδείκτες για τον πρωτοπαθή καρκίνο του παχέος εντέρου έχουν μελετηθεί εκτενώς τα τελευταία χρόνια, οι τρέχουσες κλινικές οδηγίες βασίζονται μόνο στη σταδιοποίηση της μετάστασης σε όγκους-λεμφαδένες και στην ανίχνευση ελαττωμάτων επιδιόρθωσης αναντιστοιχίας DNA (MMR) ή αστάθειας μικροδορυφόρων (MSI) (εκτός από τις τυπικές παθολογοανατομικές εξετάσεις) για τον καθορισμό των συστάσεων θεραπείας. Οι ερευνητές έχουν παρατηρήσει έλλειψη συσχέτισης μεταξύ των ανοσολογικών αποκρίσεων που βασίζονται στην γονιδιακή έκφραση, των μικροβιακών προφίλ και του στρώματος του όγκου στην ομάδα καρκίνου του παχέος εντέρου του Cancer Genome Atlas (TCGA) και της επιβίωσης των ασθενών.
Καθώς η έρευνα έχει προχωρήσει, τα ποσοτικά χαρακτηριστικά του πρωτοπαθούς καρκίνου του παχέος εντέρου, συμπεριλαμβανομένης της κυτταρικής, ανοσολογικής, στρωματικής ή μικροβιακής φύσης του καρκίνου, έχουν αναφερθεί ότι συσχετίζονται σημαντικά με τα κλινικά αποτελέσματα, αλλά εξακολουθεί να υπάρχει περιορισμένη κατανόηση του πώς οι αλληλεπιδράσεις τους επηρεάζουν τα αποτελέσματα των ασθενών.
Για να αναλύσει τη σχέση μεταξύ της φαινοτυπικής πολυπλοκότητας και του αποτελέσματος, μια ομάδα ερευνητών από το Ινστιτούτο Ιατρικής Έρευνας Sidra στο Κατάρ ανέπτυξε και επικύρωσε πρόσφατα μια ολοκληρωμένη βαθμολογία (mICRoScore) που προσδιορίζει μια ομάδα ασθενών με καλά ποσοστά επιβίωσης συνδυάζοντας τα χαρακτηριστικά του μικροβιώματος και τις σταθερές ανοσολογικής απόρριψης (ICR). Η ομάδα πραγματοποίησε μια ολοκληρωμένη γονιδιωματική ανάλυση φρεσκοκατεψυγμένων δειγμάτων από 348 ασθενείς με πρωτοπαθή καρκίνο του παχέος εντέρου, συμπεριλαμβανομένης της αλληλούχισης RNA των όγκων και του αντίστοιχου υγιούς ιστού του παχέος εντέρου, της αλληλούχισης ολόκληρου του εξονίου, της αλληλούχισης του υποδοχέα βαθέων Τ-κυττάρων και του γονιδίου rRNA των βακτηρίων 16S, συμπληρωμένης από αλληλούχιση ολόκληρου του γονιδιώματος του όγκου για τον περαιτέρω χαρακτηρισμό του μικροβιώματος. Η μελέτη δημοσιεύθηκε στο Nature Medicine ως «Ένας ολοκληρωμένος άτλαντας όγκων, ανοσοποιητικού και μικροβιώματος του καρκίνου του παχέος εντέρου».

Άρθρο που δημοσιεύτηκε στο Nature Medicine
Επισκόπηση AC-ICAM
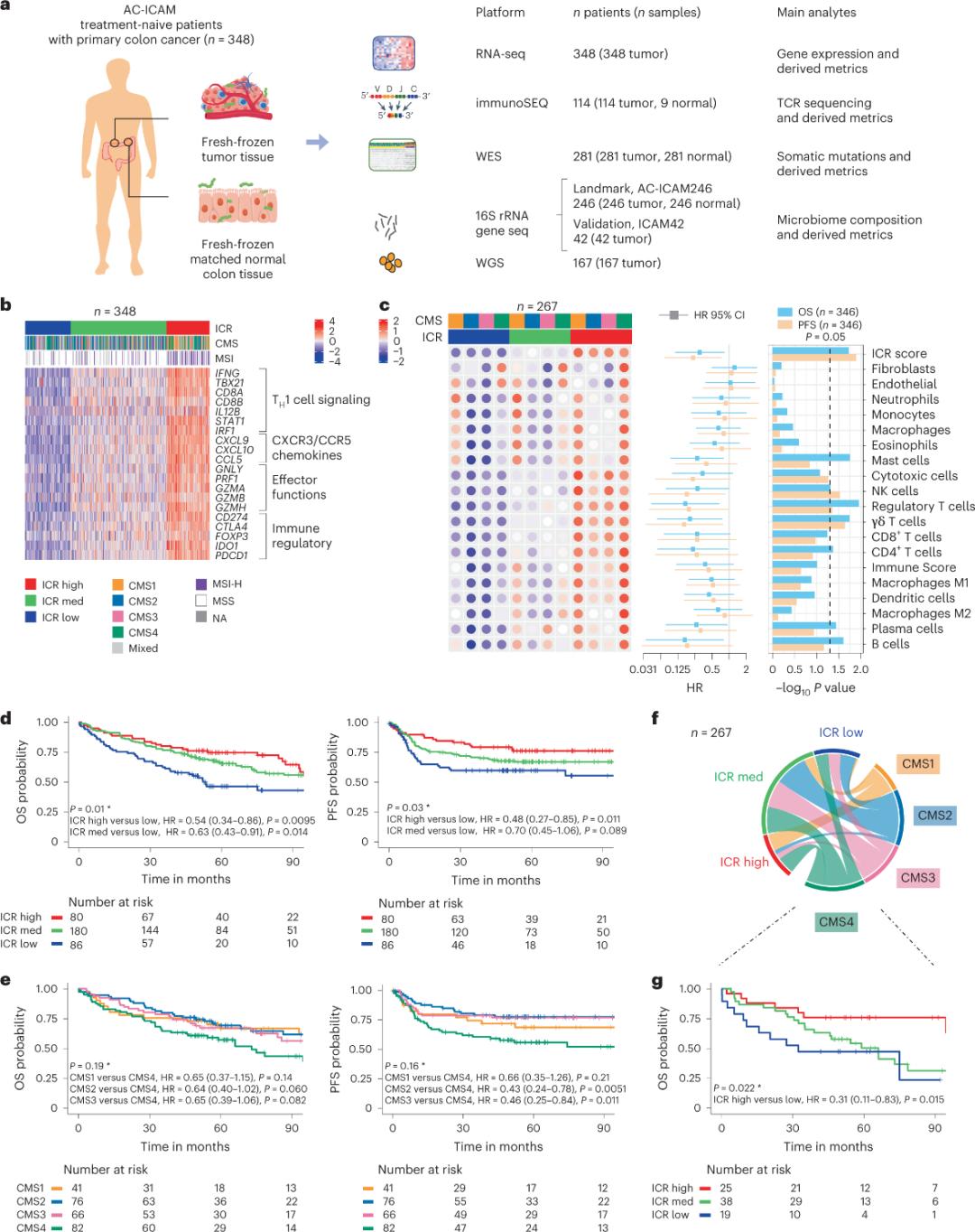
Οι ερευνητές χρησιμοποίησαν μια ορθογώνια γονιδιωματική πλατφόρμα για να αναλύσουν φρέσκα κατεψυγμένα δείγματα όγκων και αντιστοίχισαν παρακείμενο υγιή ιστό του παχέος εντέρου (ζεύγη όγκου-φυσιολογικού) από ασθενείς με ιστολογική διάγνωση καρκίνου του παχέος εντέρου χωρίς συστηματική θεραπεία. Με βάση την αλληλούχιση ολόκληρου του εξονίου (WES), τον έλεγχο ποιότητας δεδομένων RNA-seq και τον έλεγχο κριτηρίων ένταξης, τα γονιδιωματικά δεδομένα από 348 ασθενείς διατηρήθηκαν και χρησιμοποιήθηκαν για ανάλυση κατάντη με διάμεση παρακολούθηση 4,6 ετών. Η ερευνητική ομάδα ονόμασε αυτόν τον πόρο Sidra-LUMC AC-ICAM: Ένας χάρτης και οδηγός για τις αλληλεπιδράσεις ανοσοποιητικού-καρκίνου-μικροβίου (Σχήμα 1).
Μοριακή ταξινόμηση χρησιμοποιώντας ICR
Καταγράφοντας ένα αρθρωτό σύνολο ανοσολογικών γενετικών δεικτών για συνεχή ανοσοεπιτήρηση του καρκίνου, που ονομάζεται ανοσολογική σταθερά απόρριψης (ICR), η ερευνητική ομάδα βελτιστοποίησε την ICR συμπυκνώνοντάς την σε ένα πάνελ 20 γονιδίων που καλύπτει διαφορετικούς τύπους καρκίνου, συμπεριλαμβανομένου του μελανώματος, του καρκίνου της ουροδόχου κύστης και του καρκίνου του μαστού. Η ICR έχει επίσης συσχετιστεί με την ανοσοθεραπεία σε μια ποικιλία τύπων καρκίνου, συμπεριλαμβανομένου του καρκίνου του μαστού.
Αρχικά, οι ερευνητές επικύρωσαν την υπογραφή ICR της ομάδας AC-ICAM, χρησιμοποιώντας μια προσέγγιση συν-ταξινόμησης βασισμένη σε γονίδια ICR για να ταξινομήσουν την ομάδα σε τρεις συστάδες/ανοσολογικούς υποτύπους: υψηλό ICR (θερμοί όγκοι), μέτριο ICR και χαμηλό ICR (ψυχροί όγκοι) (Σχήμα 1β). Οι ερευνητές χαρακτήρισαν την ανοσολογική προδιάθεση που σχετίζεται με τους συναινετικούς μοριακούς υποτύπους (CMS), μια ταξινόμηση καρκίνου του παχέος εντέρου που βασίζεται σε μεταγραφώματα. Οι κατηγορίες CMS περιελάμβαναν CMS1/ανοσολογική, CMS2/κανονική, CMS3/μεταβολική και CMS4/μεσεγχυματική. Η ανάλυση έδειξε ότι οι βαθμολογίες ICR συσχετίστηκαν αρνητικά με ορισμένες οδούς καρκινικών κυττάρων σε όλους τους υποτύπους CMS, και θετικές συσχετίσεις με ανοσοκατασταλτικές και στρωματικές οδούς παρατηρήθηκαν μόνο σε όγκους CMS4.
Σε όλα τα CMS, η αφθονία των υποσυνόλων φυσικών φονικών κυττάρων (NK) και Τ κυττάρων ήταν υψηλότερη στους υποτύπους ICR με υψηλή ανοσία, με μεγαλύτερη μεταβλητότητα σε άλλα υποσύνολα λευκοκυττάρων (Σχήμα 1γ). Οι ανοσοποιητικοί υποτύποι ICR είχαν διαφορετική συνολική επιβίωση (OS) και επιβίωση χωρίς εξέλιξη της νόσου (PFS), με προοδευτική αύξηση της ICR από χαμηλή σε υψηλή (Σχήμα 1δ), επικυρώνοντας τον προγνωστικό ρόλο της ICR στον καρκίνο του παχέος εντέρου.
Σχήμα 1. Σχεδιασμός μελέτης AC-ICAM, υπογραφή γονιδίων που σχετίζονται με το ανοσοποιητικό σύστημα, ανοσοποιητικοί και μοριακοί υποτύποι και επιβίωση.
Η ICR συλλαμβάνει εμπλουτισμένα με όγκο, κλωνικά ενισχυμένα Τ κύτταρα
Μόνο μια μειοψηφία Τ κυττάρων που διηθούν τον ιστό του όγκου έχει αναφερθεί ότι είναι ειδικά για αντιγόνα όγκου (λιγότερο από 10%). Επομένως, η πλειονότητα των ενδοκαρκινικών Τ κυττάρων αναφέρεται ως παρευρισκόμενα Τ κύτταρα (παρευρισκόμενα Τ κύτταρα). Η ισχυρότερη συσχέτιση με τον αριθμό των συμβατικών Τ κυττάρων με παραγωγικούς TCR παρατηρήθηκε σε υποπληθυσμούς στρωματικών κυττάρων και λευκοκυττάρων (ανιχνευόμενοι με RNA-seq), οι οποίοι μπορούν να χρησιμοποιηθούν για την εκτίμηση των υποπληθυσμών Τ κυττάρων (Σχήμα 2α). Στις συστάδες ICR (συνολική και ταξινόμηση CMS), η υψηλότερη κλωνικότητα των ανοσοποιητικών TCR SEQ παρατηρήθηκε στις ομάδες ICR-high και CMS υποτύπου CMS/ανοσοποιητικές ομάδες (Σχήμα 2γ), με το υψηλότερο ποσοστό όγκων ICR-high. Χρησιμοποιώντας ολόκληρο το μεταγραφόσωμα (18.270 γονίδια), έξι γονίδια ICR (IFNG, STAT1, IRF1, CCL5, GZMA και CXCL10) ήταν μεταξύ των δέκα κορυφαίων γονιδίων που συσχετίστηκαν θετικά με την ανοσοποιητική κλωνικότητα SEQ του TCR (Σχήμα 2δ). Η κλωνικότητα του ImmunoSEQ TCR συσχετίστηκε ισχυρότερα με τα περισσότερα γονίδια ICR από ό,τι οι συσχετίσεις που παρατηρήθηκαν χρησιμοποιώντας δείκτες CD8+ που ανταποκρίνονται στον όγκο (Σχήμα 2f και 2g). Συμπερασματικά, η παραπάνω ανάλυση υποδηλώνει ότι η υπογραφή ICR καταγράφει την παρουσία εμπλουτισμένων με όγκο, κλωνικά ενισχυμένων Τ κυττάρων και μπορεί να εξηγήσει τις προγνωστικές της επιπτώσεις.
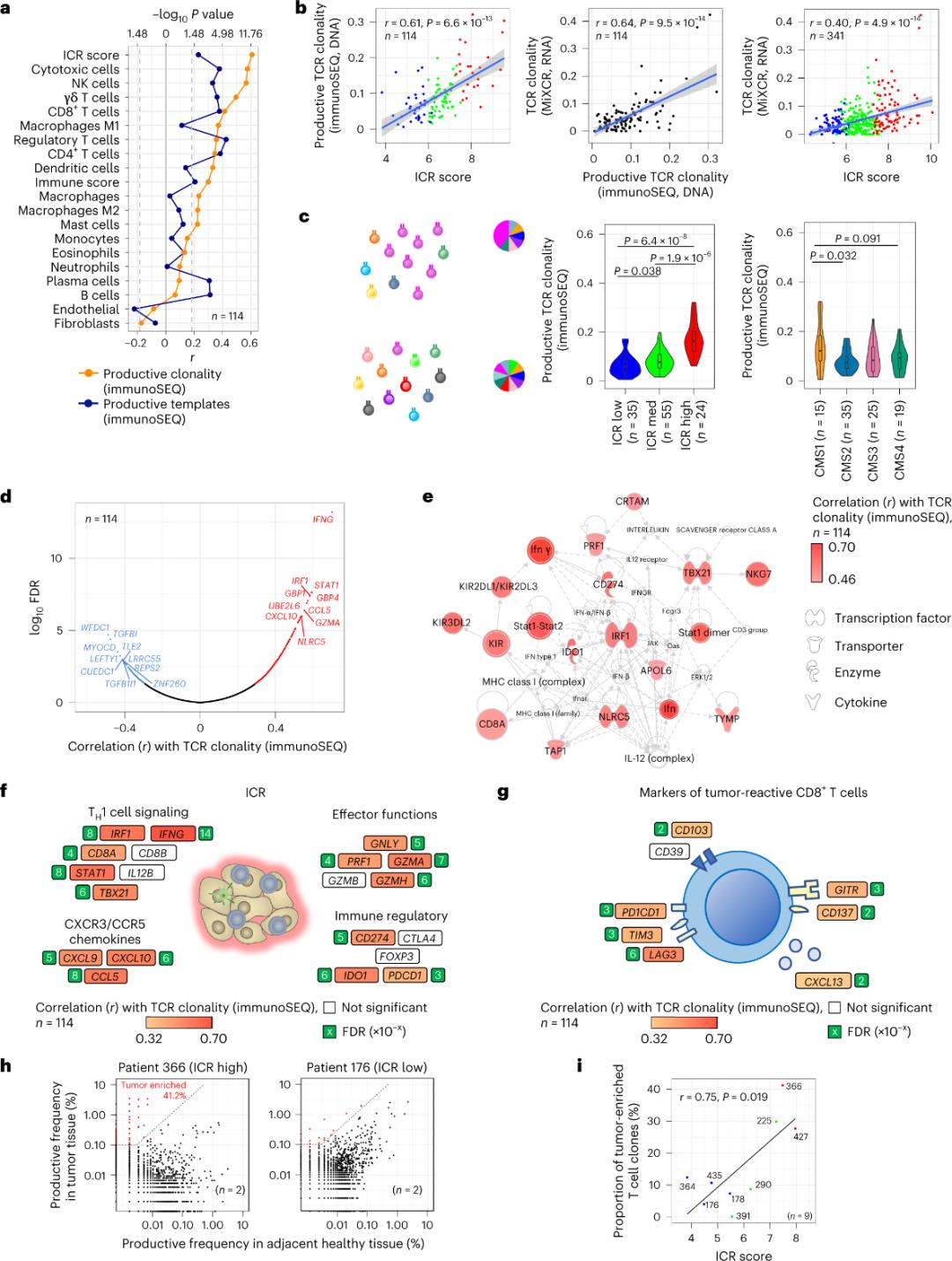
Σχήμα 2. Μετρήσεις TCR και συσχέτιση με γονίδια που σχετίζονται με το ανοσοποιητικό σύστημα, ανοσοποιητικούς και μοριακούς υποτύπους.
Σύνθεση μικροβιώματος σε υγιείς ιστούς και ιστούς καρκίνου του παχέος εντέρου
Οι ερευνητές πραγματοποίησαν προσδιορισμό αλληλουχίας 16S rRNA χρησιμοποιώντας DNA που εξήχθη από ταιριασμένο όγκο και υγιή ιστό παχέος εντέρου από 246 ασθενείς (Σχήμα 3α). Για την επικύρωση, οι ερευνητές ανέλυσαν επιπλέον δεδομένα αλληλούχισης γονιδίου 16S rRNA από επιπλέον 42 δείγματα όγκων που δεν είχαν διαθέσιμο ταιριαστό φυσιολογικό DNA για ανάλυση. Αρχικά, οι ερευνητές συνέκριναν τη σχετική αφθονία της χλωρίδας μεταξύ ταιριαστών όγκων και υγιούς ιστού παχέος εντέρου. Το Clostridium perfringens ήταν σημαντικά αυξημένο στους όγκους σε σύγκριση με τα υγιή δείγματα (Σχήμα 3α-3δ). Δεν υπήρξε σημαντική διαφορά στην ποικιλομορφία άλφα (ποικιλομορφία και αφθονία ειδών σε ένα μόνο δείγμα) μεταξύ δειγμάτων όγκων και υγιών δειγμάτων, και παρατηρήθηκε μια μέτρια μείωση της μικροβιακής ποικιλομορφίας σε όγκους με υψηλό ICR σε σχέση με όγκους με χαμηλό ICR.
Για την ανίχνευση κλινικά σχετικών συσχετίσεων μεταξύ των μικροβιακών προφίλ και των κλινικών αποτελεσμάτων, οι ερευνητές στόχευσαν στη χρήση δεδομένων αλληλούχισης γονιδίων 16S rRNA για τον εντοπισμό χαρακτηριστικών του μικροβιώματος που προβλέπουν την επιβίωση. Στο AC-ICAM246, οι ερευνητές εφάρμοσαν ένα μοντέλο παλινδρόμησης OS Cox που επέλεξε 41 χαρακτηριστικά με μη μηδενικούς συντελεστές (που σχετίζονται με τον διαφορικό κίνδυνο θνησιμότητας), που ονομάζονται ταξινομητές MBR (Σχήμα 3f).
Σε αυτήν την ομάδα εκπαίδευσης (ICAM246), η χαμηλή βαθμολογία MBR (MBR<0, χαμηλό MBR) συσχετίστηκε με σημαντικά χαμηλότερο κίνδυνο θανάτου (85%). Οι ερευνητές επιβεβαίωσαν τη συσχέτιση μεταξύ χαμηλού MBR (κινδύνου) και παρατεταμένης συνολικής επιβίωσης (OS) σε δύο ανεξάρτητα επικυρωμένες ομάδες (ICAM42 και TCGA-COAD). (Σχήμα 3) Η μελέτη έδειξε ισχυρή συσχέτιση μεταξύ των ενδογαστρικών κόκκων και των βαθμολογιών MBR, οι οποίες ήταν παρόμοιες στον όγκο και στον υγιή ιστό του παχέος εντέρου.
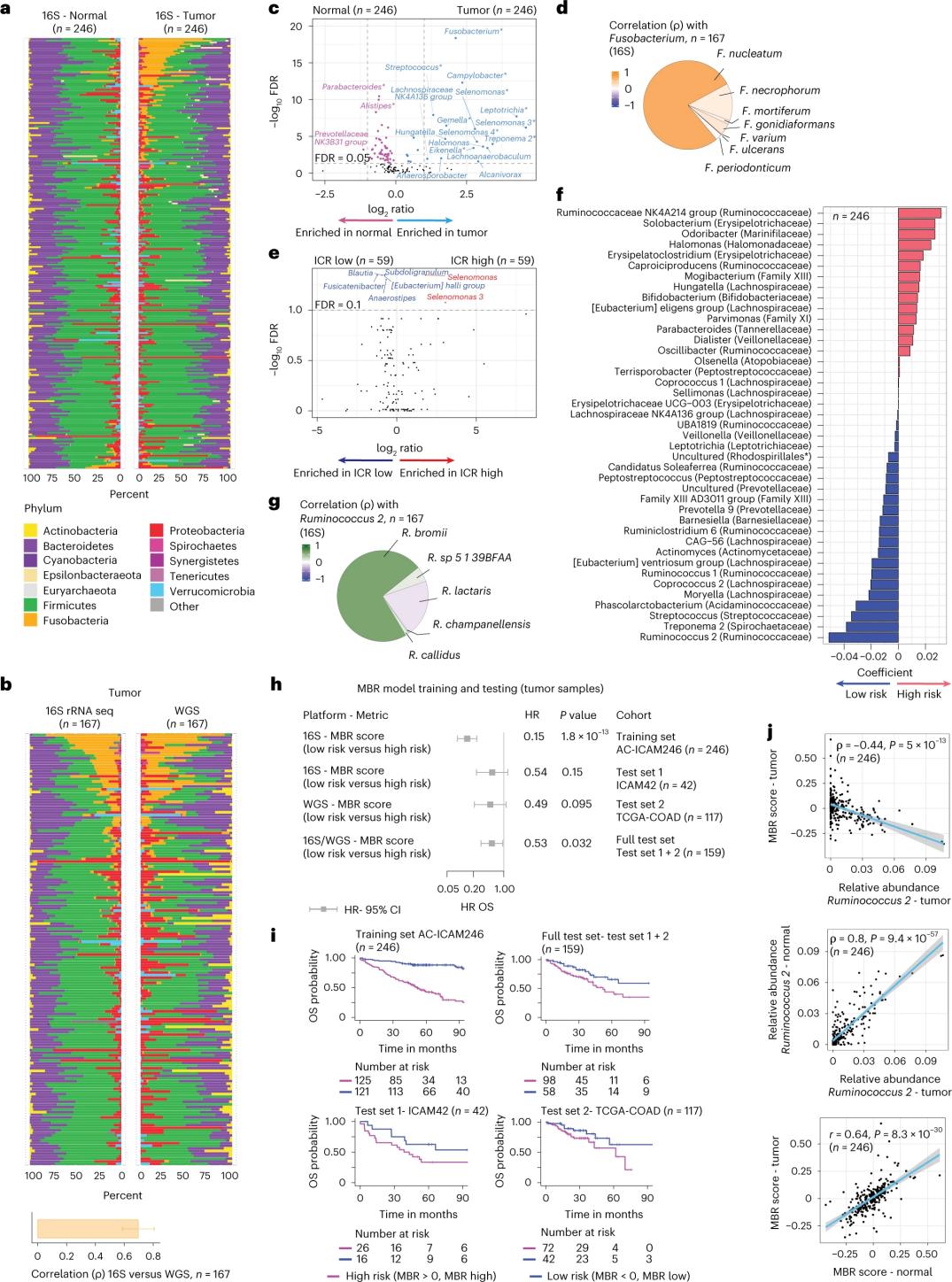
Σχήμα 3. Μικροβίωμα στον όγκο και σε υγιείς ιστούς και η σχέση του με την ICR και την επιβίωση των ασθενών.
Σύναψη
Η πολυ-ομική προσέγγιση που χρησιμοποιήθηκε σε αυτή τη μελέτη επιτρέπει την ενδελεχή ανίχνευση και ανάλυση της μοριακής υπογραφής της ανοσολογικής απόκρισης στον καρκίνο του παχέος εντέρου και αποκαλύπτει την αλληλεπίδραση μεταξύ του μικροβιώματος και του ανοσοποιητικού συστήματος. Η εις βάθος αλληλούχιση TCR του όγκου και των υγιών ιστών αποκάλυψε ότι η προγνωστική επίδραση της ICR μπορεί να οφείλεται στην ικανότητά της να συλλαμβάνει κλώνους Τ κυττάρων εμπλουτισμένους με όγκο και πιθανώς ειδικούς για το αντιγόνο του όγκου.
Αναλύοντας τη σύνθεση του μικροβιώματος του όγκου χρησιμοποιώντας αλληλούχιση γονιδίου 16S rRNA σε δείγματα AC-ICAM, η ομάδα εντόπισε μια υπογραφή μικροβιώματος (βαθμολογία κινδύνου MBR) με ισχυρή προγνωστική αξία. Παρόλο που αυτή η υπογραφή προήλθε από δείγματα όγκων, υπήρχε ισχυρή συσχέτιση μεταξύ υγιούς παχέος εντέρου και βαθμολογίας κινδύνου MBR όγκου, γεγονός που υποδηλώνει ότι αυτή η υπογραφή μπορεί να αποτυπώνει τη σύνθεση του μικροβιώματος του εντέρου των ασθενών. Συνδυάζοντας τις βαθμολογίες ICR και MBR, ήταν δυνατό να εντοπιστεί και να επικυρωθεί ένας πολυομικός βιοδείκτης φοιτητή που προβλέπει την επιβίωση σε ασθενείς με καρκίνο του παχέος εντέρου. Το πολυομικό σύνολο δεδομένων της μελέτης παρέχει έναν πόρο για την καλύτερη κατανόηση της βιολογίας του καρκίνου του παχέος εντέρου και την ανακάλυψη εξατομικευμένων θεραπευτικών προσεγγίσεων.
Ώρα δημοσίευσης: 15 Ιουνίου 2023
 中文网站
中文网站